Какво прави един генетик? С какви заболявания се занимава генетикът? Как да диагностицираме наследствени заболявания
Лекарят се занимава с откриване на наследствени заболявания и неизправности в хромозомите. Най-оптималното време за контакт с генетик е планирането на бременността, тъй като в този случай ще се извърши навременна профилактика на различни заболявания, които действат на генетично ниво. Доктор генетик ще извърши необходимата работа, за да не се стигне до прекъсване на бременността и да не се появят някои патологии.
Какво е включено в компетенциите на генетика?
По правило мандатът на генетиката включва изпълнението на редица функции - това е установяването на правилната диагноза и отчитането на наследствените черти, които се предават на генетично ниво, и изчисляването на степента на риск на един или друг, както и обяснение на всички тези фактори на семейството, което е отишло на лекар. Генетик провежда някои изследвания за семейна двойка, които включват тестове и изключват развитието на определени заболявания при детето.
С какви заболявания се занимава генетикът?
Сферата на дейност на лекар Генетиката включва огромен брой заболявания, основните от които включват следното:
- Различни заболявания, които имат автозомно-доминантен, рецесивен, Х-свързан тип наследяване;
- Всякакъв вид геномика и евгеника;
- Различни синдроми - адреногенитален, микроцитогенетичен, Wolf-Hirshhorn, Down, дисомия, котешки вик, умствена изостаналост и др.;
- Наследствени предразположения на детето към алкохолизъм, различни мутации и човешка генетика като цяло;
- В допълнение, генетик се занимава със съставяне на родословие и идентифициране на степента на риск от определено заболяване.
С какви органи се занимава генетикът?
Лекарят не лекува нито един конкретен орган, той установява природата на заболяването като цяло на генетично ниво.
Кога трябва да посетите генетик?
Препоръчително е да се свържете с генетика, ако полът на нероденото дете е много важен за родителите, както и ако семейството вече има едно дете с генетични отклонения. Също така е необходимо да кандидатствате, ако в семейството на един от съпрузите вече са родени хора с генетични заболявания, както и ако бракът е кръвно родствен.
Има и случаи на обръщане към генетиката на майки след 35 години и в случаите, когато вече е имало раждане на мъртви деца или спонтанни аборти.
Кога и какви изследвания трябва да се направят?
Когато се обърнете към генетикът, е необходимо да се подложите на серия от тестове, които ще помогнат да се идентифицира генът, който е отговорен за възникналото заболяване.
Какви са основните видове диагностика, която обикновено се извършва от генетик?
Лекарят генетик провежда редица диагностики, насочени към идентифициране на ген.
ВИДЕО
Фактът, че бебето се ражда здраво, ще бъде повлиян от околната среда, която трябва да бъде благоприятна, следователно най-доброто времеГодината за зачеването на дете е лято-есен, когато въздухът е най-свеж и растат много зеленчуци и плодове, които не са претърпели никаква обработка. Освен това през лятно-есенния период няма вирусни заболявания.
Най-благоприятната възраст за раждане на жена е между 18 и 35 години. Ако бременността настъпи по-рано или по-късно от този период, е необходимо спешно да се подложите на преглед от генетик.
Също така е много важно да имате информация, която поне по някакъв начин е свързана с медицинската история и здравето на семейството на бащата и майката на нероденото дете. Повечето двойки правят грешка, когато не използват услугите на генетик, и поради това предават някои генетични заболявания и дефекти на децата си. Много често акушерът поема част от отговорността, провеждайки разговори с множество двойки за генетични проблеми.
Най-благоприятният период за обръщане към генетик е периодът на планиране на дете и още по-добре, ако младата двойка се консултира с лекар още преди брака. Ако се случи така, че жената вече е в позиция, тогава генетикът ще предложи мерки, насочени към провеждане на пренатални тестове, които ще помогнат да се определи здравето на детето. Също така родителите ще могат да вземат окончателното решение - дали да имат деца. Много често имаше такива случаи, когато най-обикновените препоръки на генетиката спасиха двойки, които имаха висок рискдеца с патологии.
Така че всяка млада двойка трябва да се консултира с генетик, ако има риск от раждане на нездравословни деца. Също така е необходимо да се свържете с този лекар, за да предотвратите заболяването в бъдещото потомство, което ще спести младите родители от редица проблеми.
Михаил Скоблов, ръководител на лабораторията по функционална геномика в Центъра за медицински генетични изследвания, говори за това до какво в крайна сметка ще доведат изследванията в областта на медицинската генетика и защо първият „редактиран“ човек вероятно ще бъде роден в Китай.
Ще започна, като ви разкажа накратко за себе си. Повече от десет години работя в Центъра за медико-генетични изследвания, който се занимава с генетичните заболявания на човека - как са подредени, какви са причините за тях - и разработва различни подходи за тяхната диагностика и лечение. Работя и в Московския физико-технически институт, където добри условияза правене на наука. В MIPT се интересувам предимно от студенти - талантливи момчета, които вече могат да станат участници в научния процес, по-специално в процеса на помощ голяма сумаданни, които продължават да се натрупват в областта на биологията и медицинската генетика.
Какво е медицинска генетика? Едно от простите обяснения: това е наука, която се занимава с изясняване на ролята на гените за възникване на патологии при хората. Както е известно от училищния курс, цялата генетика идва от Мендел (Грегор Йохан Мендел - австрийски ботаник, августински монах, основател на теорията за наследствеността. - Рединици); и така, същите класически закони за наследяване, предписани от него, са в основата на съвременната медицинска генетика.
Да започнем с наследствените заболявания. Ще ви разкажа как са открити, как са описани, как са изследвани. Като цяло това е доста труден въпрос. Изолирайте генетични заболявания за дълго времесе провали. Това не е никак лесна задача. Но основният крайъгълен камък на медицинската генетика е разбирането на наследяването на болестите. И това се основава на така наречената генеалогия на семейството на пациента.
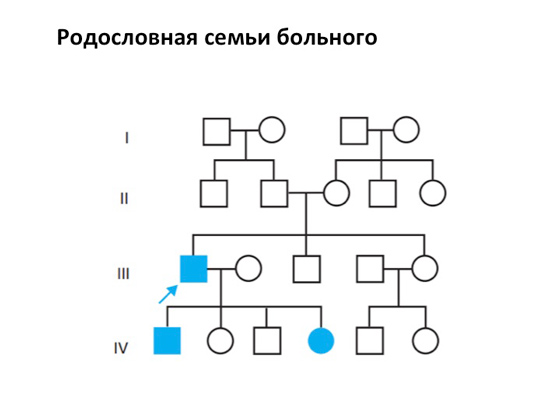
Квадратите в такива "родословия" винаги означават мъже, кръгове - жени. Тук имат деца, които също могат да дадат потомство и т.н. И в някое поколение се появява един болен член на семейството и е ясно, че болестта му по някакъв начин може да се наследи. И тук идва самият генетичен компонент, който може да бъде изолиран, боядисан и медицинската генетика вече може да започне да работи с него.
Първото изолиране на генетичния компонент се случи сравнително наскоро - през 1966 г. Имаше един учен, Виктор Алмън Маккусик, който създаде каталог на автозомно-доминантни, автозомно-рецесивни и Х-свързани фенотипове (т.е. как изглеждат хората, как се проявяват болестите в тях). И оттогава целият свят проучва и събира информация за това как изглеждат генетичните заболявания, как действат. Към днешна дата са описани много от тях - повече от осем хиляди. Има онлайн база данни OMIM (на линия менделски Наследство в човек), в която всеки учен, ако е направил компетентно изследване, може да остави запис, обогатявайки науката.
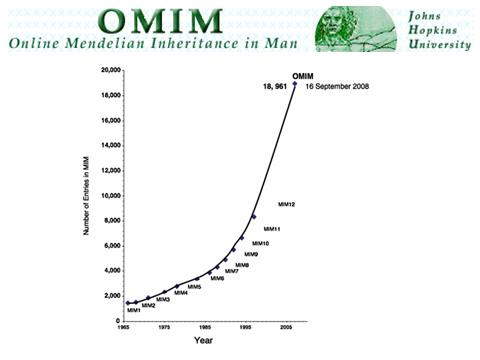
Някои болести са познати много добре – познаваме молекулярната им основа и разбираме от какво идват. За някои все още няма достатъчно информация. А за някои болести само се предполага, че могат да бъдат генетични. Но това е най-важната основа на медицинската генетика: имаме описания на заболявания, които са направени досега и те вече могат да бъдат изследвани.
Като цяло, моногенните заболявания - т.е. когато повреда в ген води до заболяване - се проявяват в ранен детство. Повечето от тях - почти 90% - се диагностицират в ранна детска възраст. По-малко от 10% се появява след пубертета и само 1% в края на репродуктивния период. Логиката е ясна: ако в генетичния материал възникне някакъв вид срив, някакъв протеин престава да функционира, тогава, като правило, проявите на този срив са видими от първите дни на живота и много често дори в утробата. Но ако се съберат всички заболявания, тогава - при моногенните заболявания, когато повреда в един ген води до едно заболяване, честотата на техните прояви е 0,36%. Ще го кажа по друг начин: от хиляда души само четирима са заплашени да бъдат собственици на генетично заболяване. Но всички тези заболявания са изследвани най-подробно. Какви са тези болести? В Русия най-често срещаните са следните:
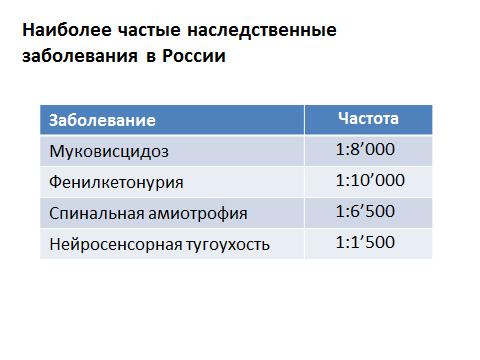
За кистозна фиброза: един пациент се среща на осем хиляди души. За фенилкетонурия: един на десет хиляди. Това е най често боледуване- също е рядкост. Но като цяло имаме доста голяма цифра.
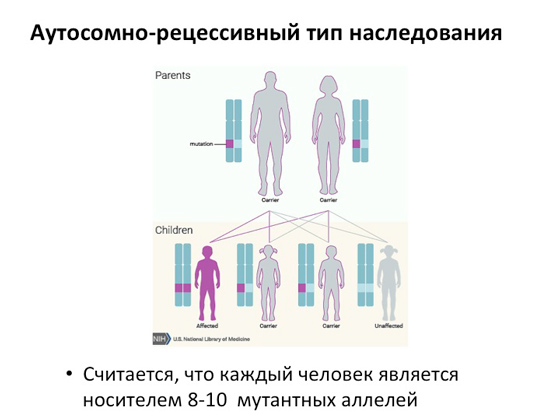
Всеки от нас има два комплекта хромозоми: единият идва от баща, другият от майка. В случай на автозомно-рецесивно заболяване, всеки от родителите може да носи генни сривове в една хромозома - едната счупване на майката, другата на бащата. Съответно, когато имат деца, са възможни три варианта: да се роди болно дете, при което са счупени две копия на гени, да се родят две деца и всяко да има по една повреда или дете, което няма нито едно счупено копие на генът. Тоест при автозомно-рецесивно заболяване в поколението само едно дете може да има и двете копия на счупените гени, в резултат на което възниква заболяването. Смята се, че средно в популацията всеки от нас може да бъде носител на осем или дори десет мутантни алела (т.е. различни формисъщият ген). Тоест, можем (не дай Боже, разбира се) да срещнем партньор, който ще има срив в същия ген и това ще доведе до факта, че децата ще се раждат според това разпределение. Автозомно-рецесивното унаследяване се среща при почти половината от всички човешки генетични заболявания.
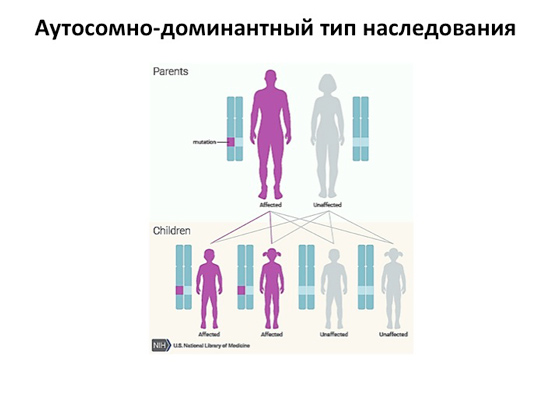
Вторият вариант е автозомно доминантен тип наследство. Тук картината е още по-проста: достатъчен е срив само в едно копие на гена и настъпва заболяване. Следователно, ако имаме един болен родител, тогава това заболяване очевидно ще бъде наследено с 50 процента вероятност от неговите деца. Защо има едно наследство, а там друго? Е, така работят гените. Понякога даден ген е толкова важен, че неговият дефицит причинява появата на заболяване. И се случва, че при децата или при самите родители половината от копията на гените са нормални, половината с мутация, но се задейства компенсаторен механизъм, който помага на тялото да се справи с това, и болестта не се развива по никакъв начин .
Откъде идват тези много повредени гени с тези мутации? Ясно е, че имаме ДНК в нашите клетки и тази ДНК е много, много голяма. Три милиарда нуклеотида! Съответно, когато клетките се делят, независимо колко прецизен е процесът на делене, възникват грешки. Въпреки факта, че имаме механизми в нашите клетки, които гарантират, че няма грешки и дори поправят неправилни замествания, част от мутациите все още се появяват и се наследяват. И дълго време не беше ясно: колко често се случва това, как работи всичко? И едва наскоро - буквално през последните няколко години - бяха публикувани няколко много силни научни труда. Геномите на здрави и болни хора бяха напълно секвенирани, за да може да се оцени как възникват нови мутации спрямо първото и второто поколение и се оказа, че средно децата наследяват около четиридесет нови промени от баща си. Тоест в генома на бащата ги няма тези изменения, но се появяват при детето. И което е най-интересното, в същите произведения се показва, че колкото по-възрастен е бащата, толкова повече щети в неговата ДНК се предават на потомството. Между другото, това не се отнася за жените. Средно около десет до двадесет замествания се предават от майка на дете, но този брой не зависи от възрастта на майката. Пак ще повторя. Въпросът е, че ако вземем двама абсолютно здрави хора и те имат дете, тогава бебето ще има около четиридесет нови замествания от бащата и двадесет нови замествания от майката, тоест то ще има около шестдесет замествания в генома, които родителите нямат.. И е ясно, че тези шестдесет промени могат да бъдат разположени навсякъде. Те може да са в някои важни гени или може да са в гени, които нямат никакъв смисъл. Но винаги има шанс тези промени все още да увредят някой ген и да причинят заболяване от автозомно-рецесивен тип или автозомно-доминантно. И с това не можем да направим абсолютно нищо - така работи природата. И тя все още е доста перфектна. Само си представете: три милиарда нуклеотида се удвояват по време на клетъчното делене и всичко това е доста сложен, голям процес и в този случай могат да възникнат само четиридесет грешки. Тези болести винаги е имало, има и ще има и човечеството не може да се отърве от тях. Но най-важното - и това е, което медицинската генетика прави, върху което се фокусира - сега имаме ДНК диагностика.
![]()
Защо се диагностицират генетични заболявания? Преди всичко, за да разбере човек съдбата си. Когато човек е болен от нещо, знанието и самото разбиране на природата на това заболяване - как протича, защо е възникнало - прави живота психологически много по-лесен. Второ и често най-много важен момент: ДНК диагностиката е необходима, за да могат чрез знанието хората да планират раждането на здрави деца. И сега ще ви разкажа как работи.
Има много генетични заболявания и причините за възникването им също са много. Първите изследвания на тези причини изглеждаха много прости: всичко, което учените можеха да направят преди 50-60 години, беше да погледнат през микроскоп и да видят как са подредени човешките хромозоми. И днес знаем, че човек има 23 чифта хромозоми. Всички възникващи аномалии по отношение на тази норма учените регистрират, описват и свързват с някакви генетични заболявания. Ето една картина, която е лесна за разбиране, ако внимателно се вгледате какво не е наред с нея.
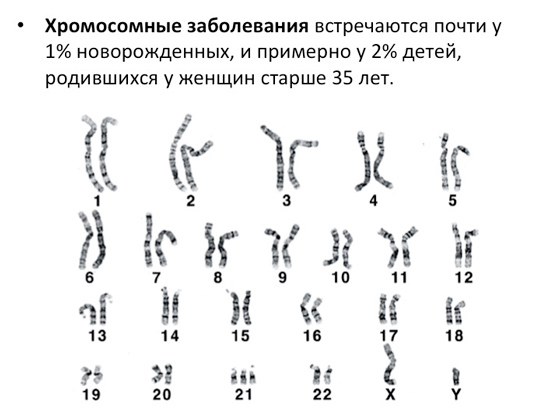
Лесно се вижда, че 21-вата хромозома има три копия вместо две. Да не го забележите в микроскоп дори за ученик е трудно. И е ясно, че подобно необичайно увеличение на копията на хромозомите - както и, напротив, намаляването - води до заболяване. Същото важи и ако хромозомата по някакъв начин е прекалено дълга или стане по-къса. Ето откъде идват хромозомните нарушения. Те представляват много голяма група - около 1% от новородените имат такива патологии (и около 2% от децата се раждат с хромозомни патологии при жени над 35; разбира се - така работи биологията - с възрастта някои процеси започват да работят по-зле , включително ембрионално развитие и много повече). Обща статистика хромозомни аномалииподредени по много интересен начин. На всеки 10 хиляди бременности, които могат да бъдат статистически анализирани, имаме около 9 хиляди с нормални хромозоми и около 800 случая с патологии. И сред тези 800 - пак така е устроена природата - само 50 случая водят до това, че се раждат деца, има някакви аномални неща. Останалите бременности, като правило, замръзват, не се развиват и завършват спонтанни аборти. От една страна, това е добре. Природата разбира, че трябва да има нормален набор от хромозоми и ако нещо не е наред - има повече, по-малко хромозоми, някои важни фрагменти се губят, - започват процеси на клетъчно ниво, които спират бременността. От друга страна, в някои случаи бременността продължава, независимо от всичко. Един от най-известните примери е тризомия 21, която води до синдром на Даун.
Разбира се, днес ги има различни начиниизбягвайте всичко това. Микроскопският метод за наблюдение на количеството и качеството на хромозомите, който съществува от много дълго време и много успешно, постепенно се заменя с по-модерен и чувствителен метод, наречен „микрочипов анализ“.
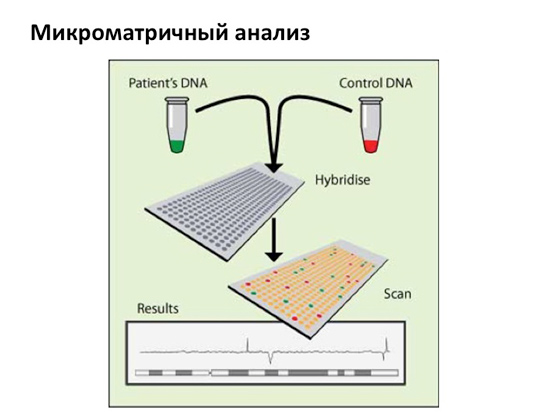
Ще опиша накратко как работи: ДНК на пациента и контролна ДНК се вземат, подготвят се по хитър начин, флуоресцентно се маркират и хибридизират върху специални матрици, в резултат на което виждаме хромозоми и виждаме флуоресцентен сигнал, който идва от различни фрагменти от пациента ДНК. В някои случаи сигналът се увеличава и това означава, че на това място се появяват копия на гени, в някои случаи, напротив, той изчезва, което означава, че е имало някакъв участък в гена, но е изчезнал. Тоест в единия случай има дублиране, в другия - изтриване. Микрочиповият анализ е много чувствителен и с негова помощ събитията могат да се видят с изключително висока точност.
Въпреки това секвенирането на ДНК е било и остава основният метод за диагностика. Той е изобретен през 1980 г. от прекрасния учен Фредерик Сангер, който измисля как да определи самите нуклеотиди, които изграждат нашата ДНК. Към днешна дата този вид анализ е пуснат в действие, прави се в почти всички лаборатории за ДНК диагностика в света. Извършва се много бързо, ефективно, с него можете да изследвате отделни участъци от гени. Грубо казано, това е основната машина на медицинската генетика. Търсенето на генни мутации с помощта на ДНК секвениране е много просто: на изхода получаваме хроматограма, където всеки изблик на сигнал е последван от специфична буква. Когато секвенираме ДНК на пациента, можем да открием това здрав човекна едно място буквата Т, а при пациента на същото място - буквата Ж. Откриването на мутации в някои специфични гени не е трудна задача. Основното е да разберете къде да търсите тези мутации.
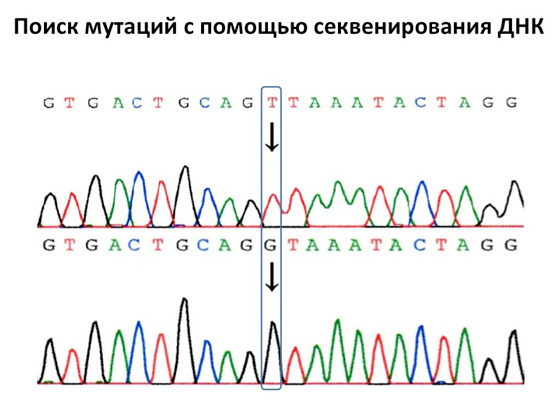
Следващата стъпка в развитието на ДНК диагностиката е масовото паралелно секвениране. Изобретени са такива мощни машини, които могат да секвенират целия ви геном наведнъж, тоест всички хромозоми, всички гени ще бъдат анализирани и дешифрирани в един анализ. Тази технология се появи сравнително наскоро и дълго време не работеше достатъчно добре. Днес всички грешки са елиминирани и масовото паралелно секвениране е един от най-точните анализи, достъпни за повечето хора. Всеки може да го направи - струва около 30 хиляди рубли. Сега машините за последователност изглеждат така:

Но най-интересното е, че те, както учените очакват (и правилно правят), ще бъдат изместени в близко бъдеще от много малки, много компактни мини секвенсори, които ще бъдат свързани към USB-порт. Тази технология в момента се тества - докато все още прави много грешки - но се очаква, че такова устройство ще струва само около $ 200 и ще изглежда по следния начин:

До известна степен много добре, но в същото време и лошо. Появата на такива технологии, способни на този вид анализ, доведе до факта, че в развитите страни - по-специално в Англия и Холандия - държавните болници направиха такъв анализ задължителен за всеки, който идва при тях. И няма значение дали човек има генетични заболявания или не: веднага щом си уговори среща с лекар, веднага му се дава секвениране на генома. Това беше въведено през 2011 г. - тоест сравнително наскоро - и сега има все повече и повече клиники, които практикуват този подход. И всичко би било добре и чудесно, но лекарят получава различни букви в ръцете си - А, Т, Ж, С, които могат да следват една след друга в различен ред, а броят на тези букви, които всеки от нас има, е около три милиарда парчета.

Най-трудната задача на този подход (секвениране на генома и неговия последващ анализ) е да дешифрира смисъла на тази последователност, да я интерпретира, да разбере къде съдържа мутации, които причиняват заболявания или предразположение към тях, и къде не. Веднага щом хората се научат да разбират това декодиране, „прочетат“ тази анотация, веднага ще започне следващият етап в развитието на медицинската генетика. Но докато това не се случи, едва ли ще бъде полезно, ако минисеквенсорите влязат в домовете ни, така да се каже.
Осъзнаването на този проблем започна с тези двама прекрасни хора. През 2007 г. бяха публикувани две работи - паралелно и почти едновременно - в които бяха секвенирани личните геноми на Крейг Вентър и Джеймс Уотсън (да, този, който откри двойноверижната структура на ДНК, наистина велик учен; като знак че е направил за наука, му е представен такъв подарък). Като цяло, тези две работи излязоха за секвениране на отделни човешки геноми, в които учените се опитаха да изолират значението на тази последователност и не успяха. Тъй като анализът откри гени, отговорни за определен фенотип (цвят на очите, цвят на косата) или отговорни за появата на някои заболявания, но всъщност тези прояви не бяха открити. Или, обратното, Вентър и Уотсън са имали заболявания и различни физиологични състояния, но нищо в "резюмето" не ги е посочило. Възникна празнина. Изглежда, че знаем буквите - A, T, G, C, но не знаем как да тълкуваме правилно значението им. Тази празнина все още съществува. Защо? Тъй като човешкият геном е много голям и ако секвенираме ДНК на някой от нас, ще се окажем с около три милиона от някои индивидуални различиякоето ще ни отличава един от друг. Какво беше направено навремето с Вентър, Уотсън и други неизвестни хора: когато бяха секвенирани, се оказа, че 3,2 милиона нуклеотида отличават Уотсън от всички останали. И все още е много, много трудно да се разбере дали тези три милиона са важни и кои характеристики са по-важни от другите. Дори ако вземем не целия геном, не цялата дълга ДНК последователност, а разгледаме само значими области, които съдържат гени, от които се образуват протеини, които изпълняват някаква функция. В генома има около един процент от такива области. Общо всички те съдържат от 30 до 70 хиляди геномни разлики. И да разберем кои влияят върху работата на протеина и кои не, от гледна точка на медицинската генетика, все още е много трудна задача. Работата бавно върви напред и отново подходът, открит в самото начало на медицинската генетика, анализът на родословието на пациента, помага за това. Когато няма нужда да се сравнява ДНК на този конкретен човек с ДНК на други хора, но може да се сравни с ДНК на роднини, тоест генетично близки индивиди. Ето ДНК на здрав брат, но на болен - каква е разликата между тях? В този случай намирането на причината за заболяването става много по-лесно.
Такива произведения са най-успешните. И ето един от тях: момчето имаше невропатия, те секвенираха генома на родителите и генома на момчето и чрез разликата между това, което родителите имат и новото, открито в детето, откриха мутация в ген SLC26A3, и стана ясно откъде идва това заболяване, дори бяха предложени начини за компенсирането му.

99% от генетичните заболявания днес са нелечими. Не можем да помогнем на хората по никакъв начин. А това, което дава медицинската генетика, е само профилактиката на болестите. Тук съм съставил толкова добре позната шарада - „невъзможно е да се предотврати излекуване“ и сега ще кажем всичко, което се вписва под заглавието, което ще излезе от шарадата, ако поставим запетая след втората дума. Тоест – „невъзможно е да се лекува, да се предупреждава“. И как предупреждават? Първият начин: ДНК-диагностика на носителството на мутации. Ето един интересен случай, който описва колко ефективен и правилен е този метод. Има такова генетично заболяване на Тай-Сакс – много тежко, много рядко. На възраст около шест месеца децата изпитват спиране на умственото и физическо развитие, зрението, слуха, способността за преглъщане постепенно се губят, детето умира на възраст около четири години. Известно е, че мутацията, причиняваща заболяването, е в гена ХЕКСАче това е автозомно рецесивен тип наследяване, тоест и двамата родители имат счупено копие на гена и детето наследява и двете счупвания. Нашето съществуване е подредено по такъв начин, че в някои страни, които живеят отделно и затворени, такива заболявания са много чести. В общи линии в случая с Tay-Sachs това е Израел. И по-специално евреите ашкенази. Едно болно дете на три хиляди новородени. Заболяването е сериозно, а Израел е държава, която се грижи за здравето на нацията. Затова на държавно ниво беше въведено задължително изследване за носителство на мутации в гена ХЕКСА, а само няколко години по-късно в Израел започва да се ражда само едно болно дете на много стотици хиляди. Подобна история беше във Финландия, която през последните 300 години беше много изолирана, не взаимодействаше много със света и това доведе до факта, че някои генетични заболявания при финландците станаха много чести. Те също въведоха програма за скрининг за носителство на няколко заболявания наведнъж - и за много кратък период от време всички те бяха активно елиминирани.
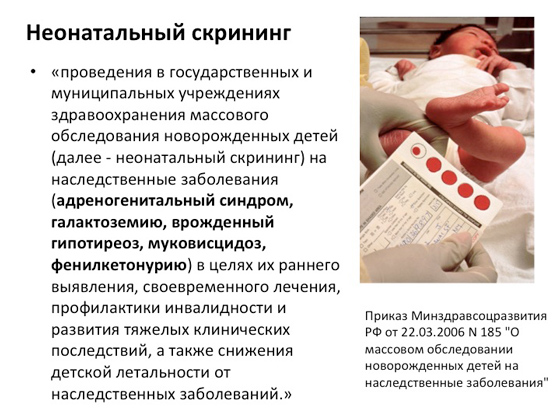
Преди няколко години в Русия също стартира програма, наречена „неонатален скрининг“. Тоест, веднага щом се роди дете, веднага се вземат няколко капки кръв от петата му и се извършва ДНК диагностика за най-често срещаните генетични заболявания у нас: адреногенитален синдром, галактоземия, вроден хипотиреоидизъм, муковисцидоза, фенилкетонурия . Всичко това се прави, за да се разбере на ранен етап как да се помогне на човек, да се компенсира възможно най-много патогенния ефект и да се предотврати неговото развитие.
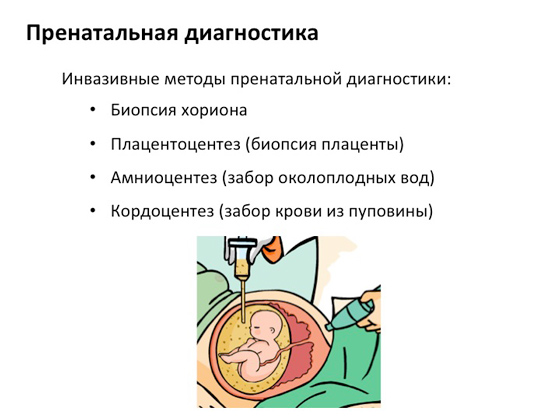
Следващата диагностична възможност е пренаталната диагностика. На ранни датибременност, внимателно, без да увреждат нито плода, нито вътрешните органи на майката, те вземат някои части от хориона, тоест мембраните на плода, които се използват за генетичен анализ на нероденото дете, за да се разбере дали той носи някакви сривове в гените си. Ако се окаже, че има сривове, на майката се дава избор дали да прекрати бременността или да продължи. Това е много важно – предлага се избор. Ето как работи генетичното консултиране: няма строги правила, човек сам решава как да живее с него.
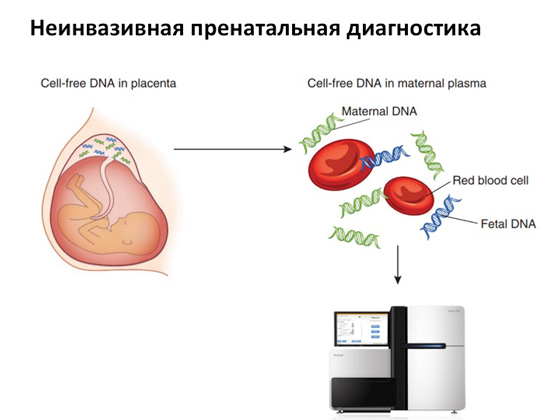
Благодарение на появата на мощни секвенатори, вече е достъпна неинвазивна пренатална диагностика. Подреден е много интересно. В ранните етапи на бременността - например на десетата седмица - се взема кръв от майката от вената. Известно е, че по време на развитието на плода част от клетките му умират, тяхното ДНК се разпада и навлиза в кръвта на майката. И ако вземете кръв от майката и използвате мощен секвенсер, тогава с помощта на специални алгоритми можете да идентифицирате коя ДНК е майчина и коя е плода и да видите дали има някакви замествания, мутации в генома на плода. И ако има мутации, тогава майката отново има право на избор.
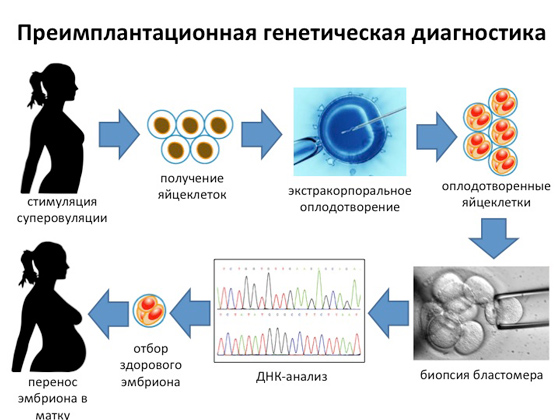
Венецът на всички трудове на днешните генетици е така наречената предимплантационна генетична диагностика. Появи се съвсем наскоро, това е най-трудният, най-отнемащият време и най-скъпият диагностичен метод, но ви позволява да получите сто процента здраво дете в по-голямата част от случаите. Веднага ще направя резервация, че такава диагноза е необходима само в случаите, когато семейна двойка идва в лабораторията и казва: първото ни дете е родено с такова и такова генетично заболяване, но искаме следващото да бъде здрави. Генетиците анализират цялата семейна история, изолират ген със специфична мутация и разбират какво трябва да се направи, така че нероденото дете да няма тази мутация. как става това При жената се предизвиква суперовулация, в резултат на което се получават определен брой яйцеклетки. След това се извършва ин витро оплождане в лабораторията. Няколко дни по-късно от оплодените яйцеклетки се избира една клетка без увреждане на бъдещия ембрион, която се използва за генетична диагностика. И ако е възможно да се получи информация, че тази оплодена яйцеклетка не съдържа никакви мутации на етапа на бластомера, тогава именно тази яйцеклетка се имплантира в майката, която след девет месеца ще даде напълно здраво потомство.
Медицинската генетика е разработила много различни подходи за създаване на условия, при които е възможно да се избегне появата на генетични заболявания, но, разбира се, в случай на нови мутации, водещи до появата на наследствени заболяванияне можем да предвидим нищо. В резултат на това се раждат болни деца. И разбирането, че те трябва да бъдат лекувани (тъй като не могат да бъдат предупредени) е много, много спешна задача. И науката също върви в тази посока. Основният проблем е, че става дума за осем хиляди заболявания. Невъзможно е дори чисто теоретично да се разработи някакъв универсален подход, който би позволил да се излекува всичко във всеки случай. Затова за всеки случай генетиците измислят индивидуални решения, индивидуални технологии.
![]()
Ето диаграма, която показва различни терапевтични стратегии, използвани за лечение на генетични метаболитни заболявания. Вижда се, че в едни случаи се прибягва до операция, в други - трансплантация на тъкан или трансплантация на костен мозък. Един процент заема генната терапия, когато се доставя здраво копие на гена. В някои случаи те се опитват да ограничат заболяването чрез диета или прием. лекарства. Като цяло има много подходи.
Що се отнася до диетата, в някои случаи тя премахва болестта почти напълно. Две добре известни заболявания са галактоземия и фенилкетонурия. Първият е нарушение на въглехидратния метаболизъм, когато ензимът, който метаболизира млечната захар, след като мутира, спира да я разгражда. Но когато се роди дете, то, разбира се, се храни изключително майчиното мляко. И в този случай неусвояването на млякото бавно води до факта, че започват да се развиват различни патологии - по-специално стомашно-чревни проблеми, цироза на черния дроб, катаракта. Всичко това се случва буквално през първите седмици и, за съжаление, доста често води до смърт. Междувременно, само чрез премахване на млякото от диетата на бебето, това вродено генетично заболяване може да бъде предотвратено от проява. Същото е и с фенилкетонурия, заболяване, което е включено в пренатален скринингв Русия. Ензимът, отговорен за метаболизма на аминокиселината фенилаланин, спира да работи, когато мутира. Но ако премахнете от храната храни, които съдържат този фенилаланин (включително някои ядки, гъби, някои млечни продукти), детето ще се развива здраво. Има обаче много малко такива истории за диети, можете да ги преброите на пръсти. Учените се опитват да подберат храна за всеки пациент, за да улеснят по някакъв начин неговото съществуване. Но всяка болест е различна и мутациите не винаги причиняват разпадане на гена и прекратяване на работата му. Понякога функцията на протеина е частично нарушена и той не работи толкова ефективно, така че е достатъчно леко да се компенсира нещо някъде - и ефектът е значителен.
Вероятно ще бъде направено в Китай - ако вече не е направено зад кулисите, което всички също обсъждат - "редактирано" лице.
Най-общо методите за лечение на наследствени заболявания могат да бъдат разделени на две групи. Първият се дължи на съединения с ниско молекулно тегло, когато можете да изберете някакво хапче, което ще компенсира съществуващите сривове. Въпреки факта, че всички сме свикнали да приемаме хапчета, в случай на наследствени заболявания това много рядко работи. Но това, което винаги трябва да работи чисто теоретично - и в случай на генетични сривове на първо място - е използването на различни молекулярни методи, където сега се движи цялата медицинска генетика. Най-интересното е, че за да се използват всички тези подходи, има цял арсенал от различни опции. Има методи, които ви позволяват да активирате работата на някои специфични гени: генът не работи и ние можем да го накараме да работи активно в тази клетка. Или, напротив, мутантен ген работи, произвеждайки токсични продукти, но има подходи, които могат селективно да потиснат неговата работа, така че той, сред цялото генно разнообразие, да спре да работи.
Най-новото и интересно нещо, което се роди в генетиката само преди пет години, е редактирането на мутантно копие на ген. Подходи, които ви позволяват да коригирате мутацията. Ще говоря за това и накъде отива всичко, но първо ще ви напомня за постулата, който всички ние, на теория, знаем - централната догма на молекулярната биология. Помните ли, говорих за великия учен Джеймс Уотсън? И така, той имаше приятел - Франсис Крик, с когото заедно откриха двойноверижната структура на ДНК. Тогава Уотсън започва да прави едни неща, а Крик - други (въпреки че и двамата работят в областта на молекулярната биология). Но по един или друг начин Крик е този, който формира тази много централна догма въз основа на структурата на молекулата на ДНК: имаме ДНК, от нея се получава РНК, от нея се получава протеин, което е връхът на цялата тази история, която тогава по някакъв начин функционира, изпълнява някои функции. Към днешна дата е описано огромно разнообразие от протеини, как са подредени, какви части имат, които отговарят за тяхното функциониране. Защо се описва това? За да се изгради след това такава огромна генна мрежа.
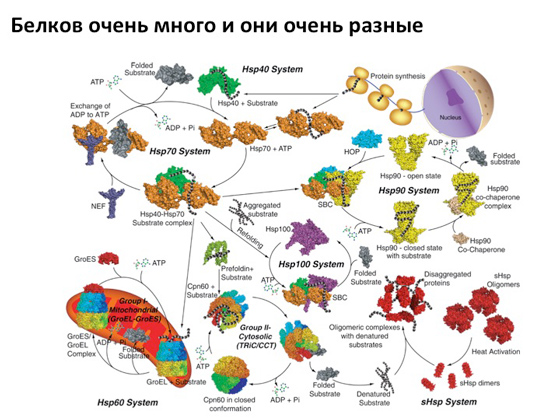
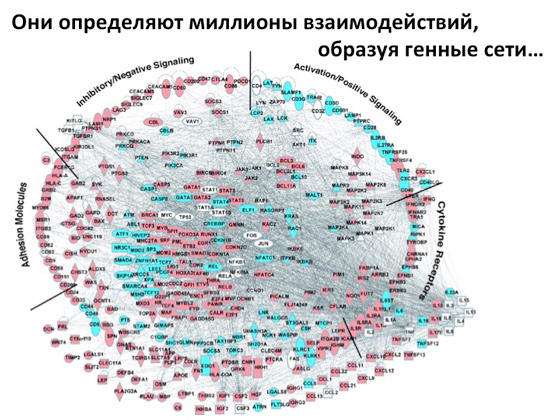
Ние разбираме кои процеси са свързани с кои гени, как се задействат тези процеси, как се предават сигнали от едно място на друго, как се регулират. Ние разбираме как да приложим всички тези подходи, за да изключим и включим някои гени. Тоест, ако се появи мутация в ген, това не означава, че всичко, в крайна сметка, не можем да направим нищо. Не, можем да разберем кой байпас да активираме, за да установим нормално съществуване на клетките, нормален метаболизъм. Или – напротив – кой път да потискаме. И фундаменталната наука е много необходима тук, за да могат тези знания да бъдат използвани по-нататък в генетиката за лечение на наследствени заболявания. Но защо е толкова трудно да се приложат тези подходи? Защото човекът е многоклетъчен организъм. Начинът, по който ме виждате сега, е милиарди клетки, всяка има своя собствена програма и всеки е ангажиран с някои от функциите си. Някои клетки в мозъка, други в мускулите. И всичко това е много сложно, така че ако възнамерявам да се намеся в някакъв процес, ще трябва да стигна не до целия организъм като цяло, а до онези клетки, които изпълняват определен фенотип. Ако пациентът страда от гърчове, тогава има лоша сигнализация в невроните и не е нужно да се намесвам в работата на всички клетки, трябва да стигна до мозъчните клетки. Съответно целенасочената доставка е най-трудната задача, пред която са изправени учените днес. Лесно се осъществява, когато има точно определен орган, добре изолиран, където всичко може да се достави безпроблемно. Най-простият пример е окото. Толкова е естествено, че е тук, толкова достъпно, толкова изолирано - и правете каквото искате с него. И с него вече се правят доста неща - включително използването на генна терапия, когато е възможно да се настроят някои процеси или, обратно, да се потиснат. Но има още един добре достъпен орган - кожата. Изглежда, че тук е, но - невъзможно е да се доставят материали там, защото кожата има защитна бариера, която не позволява никакви глупости да стигнат до там.
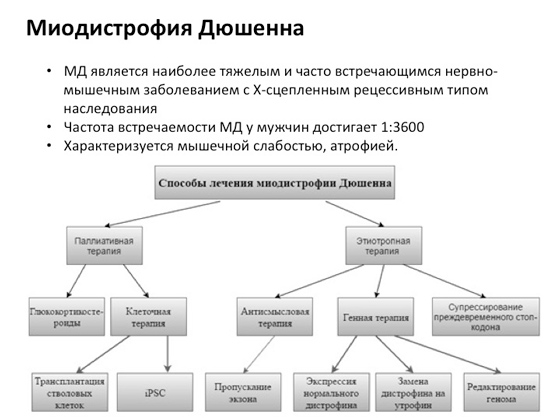
Има например такова заболяване - мускулна дистрофия тип Дюшен, което е много разпространено. За да го лекуват, учените се развиват различен видподходи. И виждате, няма един подход, върху който учените работят от много години, а много подходи. Някъде се пробва клетъчна терапия - доставят се нови клетки на пациента, за да се разбере дали ще се оправи или не. Някъде добавят различни лекарствени съединения. Някои го правят по-добре, други изобщо не го правят. Един от най-новите варианти: учените са разработили специален Химическо вещество, който избягва мутации, които причиняват появата на така наречените стоп кодони. Какво е? В някои случаи мутацията води до факта, че рибозомата, когато се движи по РНК и синтезира протеин, достига стоп кодона, който възниква поради мутацията, и в резултат на това се получава пресечен протеин вместо нормален, голям. Прекъснатият протеин не може да функционира нормално. И учените измислиха вещество, което помага на рибозомата, когато се движи по молекулата на РНК, да спре да разпознава тези стоп кодони, което води до дълъг продукт. Това всъщност е много голямо постижение - и то съвсем наскоро.
Но въпреки всичко основната история, на която всички разчитат, е генната терапия. Когато можем по някакъв начин да доставим копие на ген, който не носи никакви мутации, в клетка с мутирал ген. За това има така нареченият метод на вирусно доставяне. Тоест, самите вируси, от които се разболяваме, се модифицират по специален начин, като се премахват всички ненужни компоненти, оставя се само структурната част и се използва като транспорт за доставяне на нормален човешки ген. Тази идея е измислена много отдавна и днес се прилага в много страни едновременно. В момента се провеждат няколко хиляди съдебни процеси по целия свят.
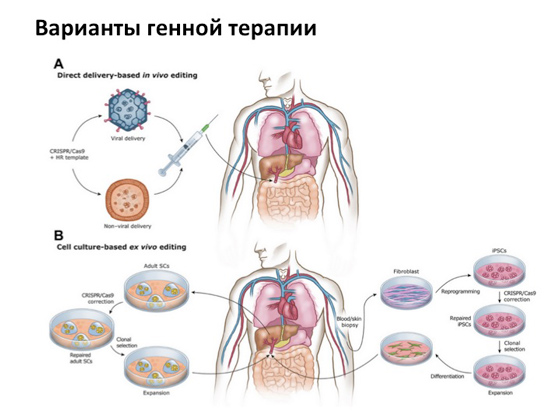
Накрая ще ви разкажа няколко хубави истории. Първият е свързан със заболяване, наречено синдром на дефицит на аденозин деаминаза. Може би сте чували за филма "Bubble Boy" (или дори сте го гледали) - за това как момчето живееше и беше в балона през цялото време, майка му го защитаваше от всичко, а той избяга от къщи и видя колко красив свят . Тази история е базирана на реални събития. Момчето се казваше Дейвид Ветър, имаше точно такова генетично заболяване, свързано всъщност с тежка форма на имунна недостатъчност. Грубо казано, детето може да умре от всяка инфекция. И когато стана ясно, че е толкова тежко болен, той беше изолиран от целия външен свят в стаите, където живееше доста дълго време. През цялото време се опитваха да го лекуват различни методи, различни лекарства. Имаше сестра, от която му направиха трансплантация на костен мозък - но и това не помогна. Историята като цяло е тъжна: момчето почина, без да живее малко преди момента, в който генната терапия беше успешно приложена за лечение на това заболяване. Изглежда така: от пациента се вземат клетки от костен мозък, които отговарят за производството на имунни клетки, с помощта на вирус им се доставя копие на гена и след това клетките се засаждат обратно на пациента. В резултат на това човек получава нов, така да се каже, костен мозък с копие на нормалния ген. Тази история е реализирана за първи път през 1990 г.
Друга история е свързана с вродената амавроза на Leber - това е дегенерация на ретината, която е доста рядка и възниква поради мутация в специфичен ген, кодиращ протеин, който отговаря за пигментния епител на ретината. Разработени са специални вирусни частици, в които има нормално копие на гена RPE65, а на пациенти, страдащи от това заболяване, са инжектирани лекарството директно в окото. В резултат на това пациенти, които са загубили зрението си или дори не са го имали от раждането, са го възстановили по време на лечението. Миналата година това генно лекарство беше одобрено от специална комисия FDA, и трябва да бъде на път да започне масова употреба.
Има много такива истории, но както си спомняте, има много наследствени заболявания, около осем хиляди.
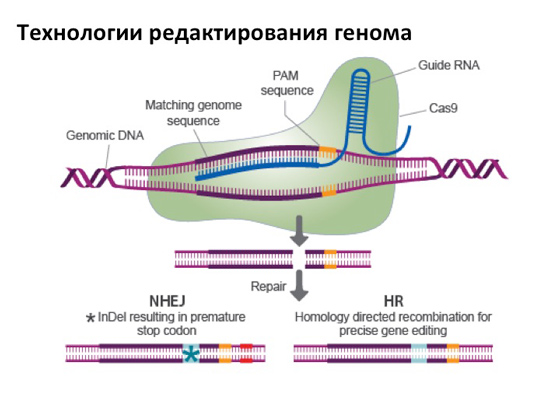
В крайна сметка, разбира се, наистина искам да кажа поне няколко думи за такава прекрасна технология като редактирането на генома. Тя направи пълен фурор в науката. Същността на това редактиране е следната: има определен вид протеин, който има нуклеазна активност, тоест той може да разделя ДНК и благодарение на една хитра РНК можем да програмираме протеина да работи така, че да разбива ДНК в конкретно място. И тогава има два варианта. Един от тях е важен за нас сега: когато протеин разруши ДНК на предварително планирано място, съдържащо мутация, могат да се активират клетъчни възстановителни механизми, позволяващи да се поправи счупването, така че да се появи ново копие на гена, което няма да носят мутацията. И създаването на този вид протеини, които могат да бъдат специфично насочени някъде, към някои специфични гени, е много важна стъпка. И в същото време много прост и удобен метод: всеки студент в добре оборудвана лаборатория може да се справи с това за няколко месеца. Ето защо сега се публикуват много публикации за това къде и кога се използва тази технология и е ясно, че на първо място те се опитват да я използват за лечение на различни генетични заболявания. И засега, съдейки по научните статии, всичко върви добре. Наскоро прочетох статия в едно списание Природата, който анализира как различни страникъм днешна дата са подредени законодателни актове и къде трябва да се появи „редактиран“ човек за първи път - няма значение, със суперсили или просто излекуван от някаква болест. Без да навлизам в подробности, абсолютно всички държави не поддържат това. Но въпросът е колко дълбоко това е заявено на законодателно ниво. Като цяло в статията се казва, че една от потенциалните страни, в които всички тези точки са по-малко ясно описани, е Китай. Освен това, ако по-рано се смяташе, че Китай е научно изостанала страна, сега те ни изпревариха така, че вече не могат да бъдат изпреварени, особено в биологията. Китайците инвестират в тази огромна сума пари. Те привличат специалисти от цял свят, изпращат свои да учат, а след това ги връщат и им дават лаборатории и институти. Те са много активни в тази посока. Вероятно в Китай ще бъде направен "редактиран" човек - ако вече не е направено зад кулисите, което всички също обсъждат. И първата история, която дълго време не можеше да бъде публикувана, беше за това, че вече са демонстрирали метод за редактиране на генома на човешки ембриони. Там нямаше нищо страшно, всичко беше направено много добре и правилно, човешките ембриони не можеха да се възпроизвеждат по-нататък и бяха взети като модел. Като цяло експериментът показа, че при редактиране има много грешки. Както е обичайно в научната общност, всяка новина от този вид се обсъжда активно: от една страна, всички разбират, че да, всички тези технологии, които току-що се появиха, са подходящи за решаване на различни проблеми. От друга страна, странични ефектикоито могат да се появят, никой не може да предвиди. И затова учените много внимателно, стъпка по стъпка, се опитват да проверят и изследват всичко това. Мразя да ви давам надежда, но ми се струва, че през следващите десет до двадесет години определено ще имаме надеждни средства за лечение с генна терапия. Засега имаме каквото имаме.
Публикувано от Наталия Кострова
Генетикът изпълнява две основни функции. Първо, той "помага" на колегите си да "диагностицират", използвайки специални генетични методи в диференциалната диагноза, и, второ, той определя "прогнозата за здравето на бъдещото потомство" (или вече родено). В същото време пред лекаря винаги възникват медицински, генетични и деонтологични проблеми; на различните етапи от консултирането преобладава едното или другото.
Медико-генетичната консултация се състои от 4 етапа; диагноза, прогноза, заключение, съвет. В същото време е необходима откровена и приятелска комуникация между генетика и семейството на пациента.
Консултирането винаги започва с изясняване на диагнозата на наследствено заболяване, тъй като точната диагноза е необходима предпоставка за всяка консултация. Лекуващият лекар, преди да насочи пациента към медико-генетична консултация, трябва, използвайки наличните за него методи, да изясни диагнозата, доколкото е възможно, и да определи целта на консултацията.
Също така е необходимо да се използват генеалогични, цитогенетични, биохимични и други специални генетични методи (например за определяне на връзката на гените или използване на молекулярно-генетични методи и др.). В такива случаи пациентът се насочва за медико-генетична консултация и генетикът съдейства на лекуващия лекар за поставяне на диагнозата. В този случай може да се наложи насочване на пациента или неговите близки за допълнителни изследвания.
Генетикът поставя на други лекари (невролог, ендокринолог, ортопед, офталмолог и др.) конкретна задача - да разпознаят симптомите на предполагаемо наследствено заболяване при пациент или неговите роднини. Самият генетик не може да бъде толкова "универсален" лекар, че да знае напълно клиничната диагноза на няколко хиляди наследствени заболявания. На първия етап от консултирането генетикът е изправен пред много чисто генетични задачи (генетична хетерогенност на дадено заболяване, наследствена или новопоявила се мутация, екологична или генетична обусловеност на дадено вродено заболяване и др.), за които той се подготвя в процеса на специализация. Изясняването на диагнозата в медико-генетична консултация се извършва с помощта на генетичен анализ, който отличава генетика от другите специалисти. За тази цел генетикът използва генеалогични, цитогенетични и молекулярно-генетиченметоди, както и анализ на генна връзка, методи на генетика на соматични клетки. От негенетичните методи широко се използват биохимични, имунологични и други параклинични методи, които подпомагат поставянето на точна диагноза. "Генеалогичният метод", при условие, че родословието е внимателно събрано, дава определена информация за диагностициране на наследствено заболяване. В случаите, когато става дума за все още неизвестни форми, генеалогичният метод ни позволява да опишем нова форма на заболяването. Ако видът на наследството е ясно проследен в родословието, тогава е възможно консултиране дори при неопределена диагноза. (Характеристиките на използването на клиничния генеалогичен метод и неговите разрешаващи възможности бяха обсъдени по-горе.) В медицинската генетична консултация този метод се използва във всички случаи без изключение. „Цитогенетично изследване“, както се вижда от опита на много консултации, се използва в поне 10% от консултациите. Това се дължи на необходимостта от прогноза за потомството с установена диагноза хромозомна болест и изясняване на диагнозата при неясни случаи с рожденни дефектиразвитие. Всички тези проблеми често се срещат в практиката на консултиране. По правило се изследват не само пробандите, но и родителите.
Биохимичните, имунологичните и други параклинични методи не са специфични за генетичното консултиране, но се използват толкова широко, колкото и при диагностиката на ненаследствени заболявания. При наследствени заболявания често се налага същите изследвания да се прилагат не само на пациента, но и на други членове на семейството (съставяне на биохимично или имунологично "родословие"). В процеса на генетично консултиране често възникват нови нужди от допълнителни параклинични изследвания. В такива случаи пациентът или неговите близки се изпращат в съответните специализирани институции. В крайна сметка диагнозата в медико-генетичната консултация се изяснява чрез генетичен анализ на цялата получена информация, включително (ако е необходимо) анализ на данни за генно свързване или резултати от изследване на култивирани клетки. За извършване на генетичен анализ е необходимо генетикът да е висококвалифициран специалист в областта на медицинската генетика. След изясняване на диагнозата се определя "прогнозата за потомството". Генетикът формулира генетичен проблем, чието решение се основава или на теоретични изчисления, използващи методите на генетичен анализ и статистика на вариациите, или на емпирични данни (емпирични таблици на риска). От това става ясно, че обичайната медицинска подготовка на общопрактикуващия лекар не му позволява компетентно да направи такава прогноза. Грешка на лекар с неправилна прогноза за семейството може да бъде фатална: тежко болно дете може да се прероди. В случаите, когато се използва пренатална диагностика, необходимостта от решаване на генетичен проблем отпада. В такива случаи не се прогнозира раждането на дете с болестта, но заболяването се диагностицира в плода. „Заключение на медико-генетична консултация и съвети на родители” като последните два етапа могат да се комбинират.
Писменото мнение на лекаря-генетик е задължително за семейството, така че членовете на семейството могат да се върнат към обмисляне на ситуацията. Заедно с това е необходимо устно да се обясни значението на генетичния риск в достъпна форма и да се помогне на семейството да вземе решение. Последните етапи на консултирането изискват най-голямо внимание. Без значение как се подобряват методите за изчисляване на риска (емпирични или теоретични), колкото и пълно да се въвеждат постиженията на медицинската генетика в работата на консултациите, е невъзможно да се постигне желаният ефект от консултирането, ако пациентите не разбират обяснението на генетик. Контактът със семеен лекар, на когото съпрузите имат особено доверие, също може да помогне тук, така че координацията на действията на семейния (лекуващ) лекар и генетика е много важна. За да се постигне целта на консултацията, при разговор с пациенти трябва да се вземе предвид нивото на тяхното образование, социално-икономическото положение на семейството, структурата на личността и отношенията на съпрузите. Много пациенти не са подготвени да възприемат информация за наследствени заболявания и генетични модели. Някои са склонни да се чувстват виновни за случилото се нещастие и страдат от комплекс за малоценност, други доста сериозно се доверяват на прогнози, базирани на „разкази на познати“, трети идват на консултацията с нереалистични искания или очаквания поради факта, че не са били наясно на възможностите за генетично консултиране (понякога включващо лекари). Трябва да се има предвид, че почти всички консултантски съпрузи искат да имат дете (иначе не биха потърсили съвет). Това значително повишава професионалната отговорност както на лекуващия лекар, така и на генетиката. Всяка неточна дума може да се тълкува в "посоката", в която са настроени съпрузите. Ако съпрузите се страхуват много да имат болно дете и, разбира се, искат да имат здраво, тогава всяка небрежна фраза на лекаря за опасността увеличава този страх, въпреки че в действителност рискът може да е малък. Понякога, напротив, желанието да имат дете е толкова силно, че дори при висок риск съпрузите решават да имат деца, защото лекарят каза за някаква вероятност за раждане здраво дете. Начинът, по който се тълкува рискът, трябва да се адаптира към всеки отделен случай. В някои случаи трябва да говорим за 25% шанс да имаме болно дете, в други - за 75% шанс да имаме здраво дете. Въпреки това винаги е необходимо да се убеждават пациентите в случайното разпределение на наследствените фактори, така че да бъдат освободени от собствената си вина за раждането на болно дете. Понякога това чувство е много силно. Препоръчително е съпрузите да се изпращат на медицинско генетично консултиране не по-рано от 3 месеца след диагностицирането на наследствено заболяване, тъй като през този период се извършва адаптация към ситуацията, възникнала в семейството, и по-рано всяка информация за бъдещи деца се възприема слабо. . Тактиката на генетика за подпомагане на пациентите да вземат решения не е окончателно определена. Разбира се, зависи от конкретната ситуация. Въпреки че решението се взема от самите пациенти, поведението на лекаря може да бъде различно: 1) ролята на лекаря при вземането на семейни решения може да бъде активна; 2) ролята на лекаря трябва да се сведе само до обяснение на значението на риска. Според нас генетик и лекуващ лекар (особено семеен лекар) трябва да помогнат със съвет при вземането на решение, тъй като при съществуващото ниво на познания в областта на генетиката сред населението е трудно за консултантите да направят самостоятелно решение. Медицинските задачи на консултирането са по-лесни за решаване от социалните и етични проблеми. Например, няма съмнение, че по-трудно наследствено заболяване, толкова по-спешно лекарят трябва да препоръча отказ от раждане. Но при едно и също заболяване, при една и съща вероятност за раждане на болно дете, различните ситуации в семейството (сигурност, отношения между съпрузи и т.н.) изискват различни подходи за обяснение на риска. „Във всеки случай решението за деца остава в семейството. 10.3.3. Организационни въпроси При организирането на медицински генетични консултации като структурни подразделения е необходимо да се разчита на системата на здравеопазване, която се е развила в страната, и да се вземе предвид степента на развитие на медицината като цяло, включително нивото на познаване на генетиката от лекар. Консултациите функционират като неразделна връзка в съществуващата система медицински грижинаселение. В повечето чужди страни с развито здравеопазване системата за консултиране е 3-степенна: 1) прогнозата за потомство в прости случаи се определя от семейния лекар; 2) по-сложните случаи "стигат" до генетик, работещ в голям медицински център; 3) консултирането в сложни генетични ситуации се извършва в специални генетични консултации. За прилагането на тази като цяло ефективна система е необходимо, от една страна, всяко семейство или лекуващ лекар да има добро разбиране на клиничната генетика, а от друга страна, нивото на организация на медицинските грижи за населението трябва да бъде високо . Медико-генетичните консултации като структурни звена на лечебните заведения могат да бъдат общи и специализирани.
Анализът на контингента на кандидатстващите за "обща консултация" според "нозологичния принцип" показва, че пробандите имат голямо разнообразие от патологии. Тъй като работата по уточняване на диагнозата в консултацията има голям дял, разнообразният профил на заболяванията на пробандите налага включването на пробандите и близките им в прегледа от различни специалисти. В тази връзка е най-целесъобразно да се създадат генетични консултации на базата на големи мултидисциплинарни медицински институции на републиканско или регионално подчинение. Пациентът и неговите близки в този случай имат възможност да получат съвет от специалисти и при необходимост ще могат да бъдат хоспитализирани. Освен това консултацията трябва да може да изпраща за специализирано (томография, хормонален профил и др.) изследване в други институции, ако болницата, на базата на която работи консултацията, няма такива възможности. Тесен контакт с други отдели и правилното им подчинение са важен принципработата на медико-генетична консултация с общ профил. В големите специализирани болници могат да се организират "специализирани медико-генетични консултации", в които генетикът придобива опит в консултирането на наследствени заболявания от един профил. В трудни случаи пациентите трябва да бъдат насочени от обща консултация към специализирана консултация. Две консултации - обща и специализирана - могат да функционират паралелно, без да се заместват една друга и да не са в подчинение. Персоналът на общата консултация трябва да включва генетици, цитогенетици и генетични биохимици. Генетикът, който провежда прием на населението, трябва да има цялостно генетично обучение, тъй като трябва да решава голямо разнообразие от генетични проблеми. Спецификата на работата на генетика се състои в това, че обектът на неговото изследване е семейството, а пробандът е само "стартовият" човек в това изследване, оттук и специфичните форми на работа. Всяка консултация изисква събиране на информация за роднини, а понякога и тяхното изследване. Заключението на генетика за повторния риск от заболяването е предназначено директно за семейството, което е поискало помощ, така че значението на заключението трябва да бъде обяснено в достъпна форма (често на няколко членове на семейството). Всичко това отнема много повече време, отколкото приемането на пациента от всеки друг специалист. Първичният преглед на пробанда и неговите родители, както и събирането на фамилна анамнеза отнема 11/2 - 2 часа. Повторната консултация (писмено мнение, обяснение в достъпна форма, помощ при вземане на решение) отнема средно 30 минути. Така един генетик може да прегледа не повече от 5 семейства за един работен ден. От всички специални изследвания най-голяма е необходимостта от цитогенетични анализи. Голямата необходимост от използването на цитогенетичния метод се дължи на насочването към медицинско генетично консултиране, преди всичко, на пациент с хромозомна патология, вродени малформации и акушерска патология. В този случай по правило не се изследва един човек, а двама или трима. Необходимостта от биохимични изследвания е около 10%, т.е. за всяко 10-то семейство, подали заявка за консултация. Това е доста висока цифра. Въпреки това, при голямо разнообразие от наследствени метаболитни заболявания, повторното използване на едни и същи биохимични методи при консултации ще бъде много рядко. Ето защо в големите градове е най-целесъобразно да се създадат специализирани биохимични лаборатории с широки методологични възможности за изследване на пациенти с различни метаболитни нарушения. В самата медико-генетична консултация се извършва "скринингова диагностика" (такива методи са "адаптирани" за широка практика) без изясняващия етап, който беше споменат по-горе. По този начин генетичната консултация като структурно подразделение е малка част от поликлиничната служба, състояща се от кабинет на генетика, процедурна зала (вземане на кръв) и лаборатория за цитогенетични и скринингови биохимични изследвания; Извършват се клинични, параклинични, молекулярно-генетични, биохимични, имунологични и други изследвания в специализирани лаборатории и лечебни заведения, към които е прикрепена консултацията. Наличието на такива консултации в болниците не изключва организирането на високоспециализирани медико-генетични центрове с всички необходими отделения.
Най-големите перспективи в науката сега се отварят на кръстопътя на научни дисциплини. Очевидно: нито един физик, астроном или химик не може без математика. Взаимодействието на атомите и молекулите може да се разглежда както от физична, така и от химична гледна точка.
Какво е екология и какво е генетика е приблизително ясно за всички. Човешкият генетичен апарат, подобно на другите жители на Земята, се влияе от различни фактори на околната среда. Освен това хората се считат за един от най-чувствителните към подобни въздействия видове.
Влиянието върху наследствеността на йонизиращото лъчение е радиационна генетика.
Генотоксикологияизучава промените в гените под въздействието на химикали.
Организмите и видовете си взаимодействат, което не минава безследно за техния генетичен апарат – обаче, както и за самата екологична генетика; съответният му раздел се нарича донякъде тромав: генетика на междуорганизмовите и междувидовите взаимодействия.
Вътре в него има дори такова интересно нещо като симбиогенетика - генетиката на взаимодействието на видове, живеещи в симбиоза.
Влиянието на Чернобил и наркотиците
Екологичният генетик се занимава не само с фундаментални изследвания в изследователски институти - той ще намери приложение и в конкретна практика. Има върху какво да се работи. Тази година се навършват 20 години от паметната авария в атомната електроцентрала в Чернобил и наистина мащабът на употребата на радиоактивни вещества вече е голям. В допълнение, лекарства и други нови вещества, независимо дали са получени от естествени източници или са изкуствено синтезирани, също трябва да бъдат тествани за мутагенност. И за да се решат много въпроси на съвременната екология, са необходими квалифицирани специалисти, които притежават както генетични методи, така и знания за взаимодействието на организмите с околната среда на различни нива.
Работейки в някоя от тези области, се занимава професионалист тестванеспецифични фактори на околната среда - тоест установява как този фактор и в каква доза влияе върху живия организъм, неговите хромозоми и гените в тях. Или провежда изследване - установява влиянието на този конкретен фактор в тази конкретна доза в този конкретен случай.
И така, какво правят с мишките?
 Тестовете са не само психологически, но и токсикологични. Токсикологичните генетици идентифицират мутагенни (когато гените мутират или хромозомната ДНК се разпада) и канцерогенни ефекти различни вещества. За тези цели има различни тестове и тестови системи. В случай, че е необходимо бързо да се направи първоначална оценка на ефекта на веществото върху организма и неговия геном (т.е. върху съвкупността от наследствени черти), се използват краткосрочни тестове. Разбира се, те не са толкова надеждни, колкото дългосрочните тестове, чиито недостатъци са високата цена на тестването и по дефиниция продължителността. Затова най-често се използват междинни тестове.
Тестовете са не само психологически, но и токсикологични. Токсикологичните генетици идентифицират мутагенни (когато гените мутират или хромозомната ДНК се разпада) и канцерогенни ефекти различни вещества. За тези цели има различни тестове и тестови системи. В случай, че е необходимо бързо да се направи първоначална оценка на ефекта на веществото върху организма и неговия геном (т.е. върху съвкупността от наследствени черти), се използват краткосрочни тестове. Разбира се, те не са толкова надеждни, колкото дългосрочните тестове, чиито недостатъци са високата цена на тестването и по дефиниция продължителността. Затова най-често се използват междинни тестове.
Освен това обикновено се провежда не един тест, а набор от три или повече различни теста и с използване на различни моделни обекти, като например мишки. В зависимост от получените резултати се прави заключение за вредата или относителната безопасност на тестваното вещество. Контролната група, разбира се, се състои от същите "обекти", но без влиянието на тестваното вещество. Индикаторът за вреда обикновено е оцеляване на моделни обекти.
По време на тестовете се изчислява и честотата на поява на злокачествени тумори и мутации при опитни животни. Уви, всеки експериментален биолог (каквито обикновено са екологичните генетици) трябва незабавно да се примири с това тъжно обстоятелство: то ще съпътства работата му. Колкото и да съжаляваме мишките, плъховете или жабите, те трябва да бъдат пожертвани, за да не станем по-късно жертви. Мога само да утеша особено впечатлителните читатели с факта, че в Лвов е издигнат паметник на Жабата, в Санкт Петербургския държавен университет - паметник на Котката, а в Научния институт по експериментална медицина (Петербург) - паметник на Кучето. .
Какви конкретни тестове се провеждат, от какви задачи се състоят работните дни? Ден след ден токсикологът-генетик провежда рутинен метафазен анализ- маркира хромозомите със специално багрило, след което самите хромозоми и съответно много от техните пренареждания (това е обект на изследване) могат да се наблюдават под микроскоп. Под наблюдението на учен са също микронуклеарни тестове(когато една клетка се дели, анормалните хромозоми, сигнализиращи за заболяване, често отиват в така наречения „микронуклеус“, който е много по-малък от нормалното клетъчно ядро; при определени условия и оцветяване с багрила, тези микроядра могат да се наблюдават върху препаратите). Има ли още анателофазен тест; основава се на факта, че някои хромозомни аномалии им пречат да се разпръснат правилно и своевременно в нови ядра по време на клетъчното делене, поради което в по-късните етапи на делене могат да се наблюдават характерни отклонения на деленето - например джъмпери или закъснения.
Ако изследвано вещество е показало намален процент на преживяемост, повишен риск от мутация или поява на злокачествени тумори при поне един от тестовете, то вече се счита за опасно.
Погледнете през микроскопа - и ми кажете дали е имало радиация
радиационна генетикасе занимават с изследване на ефекта върху генома на йонизиращото лъчение - тоест лъчение с достатъчно висока енергия, за да предизвика йонизация на молекулите. Не забравяйте, че ДНК се състои от две вериги, обвързан приятелс приятел? Част от една такава верига може да бъде синтезирана изкуствено. Тогава този т.нар сонданеобходимо е да се маркира по специален начин и след това да се „хибридизира“ със съществуващия препарат от кръвни лимфоцити. Нашата сонда ще се „свърже“ към желания ген или регион на хромозомата, сякаш е част от „нативната“ втора верига на ДНК и този регион може да се види благодарение на етикета. По този начин ще могат да се проследяват специфичните за облъчването хромозомни пренареждания. Тъй като това изследване се провежда на ниво клетка, този метод - така се нарича
in situ хибридизация- отнася се за цитогенетични. Всички горепосочени тестове обаче са и цитогенетични. Изследванията се извършват и на друго ниво – на ниво молекули.
Но във всеки случай учените гледат как се държат хромозомите. Например, знаете ли, че появата в клетка на хромозома с две центромери (обикновено стеснение, свързващо "раменете" на хромозомата, или центромер, трябва да е едно) е почти сигурно показателно за експозиция? Спонтанно такива хромозоми са изключително редки. Следователно, така наречената дицентрична хромозома служи като вид алармен сигнал за хората, участващи в радиационната диагностика. Смята се, че по броя на същите дицентрични хромозоми може приблизително да се определи получената доза радиация. На това се основава биодозиметрията.
Генетиката на привлекателността
 Генетика на междуорганизмовите взаимодействия, симбиогенетиката изследва взаимодействието на геномите на различни организми и техните видове.
Генетика на междуорганизмовите взаимодействия, симбиогенетиката изследва взаимодействието на геномите на различни организми и техните видове.
Има няколко удобни модела за такива изследвания. Една от най-достъпните е системата за взаимодействие с дрожди ( Sacharmyces cerevisia) и плодовата мушица. Drosophila melanogaster. Мухата се нуждае от стероидни хормони за нормално развитие и способност да оставя потомство - но тя не ги произвежда сама. Тя намери изход благодарение на маята. Мухата ги консумира заедно със стероидите, които те синтезират! Генотипът на дрождите влияе върху мухите - определени "семейства" дрожди, характеризиращи се със строго определен набор от гени, мухите "харесват" повече от други, те са по-ефективни, а някои дори могат да бъдат вредни за мухите.
В допълнение към мухите с дрождите се изследва и генетиката на взаимодействието на нодулните бактерии с бобовите растения (бактериите причиняват образуването на тумори върху техните корени, така че може би някои открития в тази област са приложими в онкологията - по един или друг начин, и благодарение на тях вече е открит нов начин за генетична модификация на растенията); ендо- и екзомикориза; лишеи (генетично интересна тясна комбинация от гъби и водорасли в един организъм). Тук има още много за изследване и изясняване.
Освен това има още един интерес Питай. Тъй като все повече и повече става известно, феромоните участват в избора на брачни партньори. Дори дрождите отделят феромонни вещества - и по този начин две клетки от дрожди с различни така наречени "типове чифтосване" (подобно на пола при по-високо развитите същества) се намират една друга, за да продължат своя жизнен цикъл. Във висшите организми също участва имунната система. Колкото повече различни набори от специални молекули (т.нар. основен комплекс на хистонова несъвместимост) се различават при различните индивиди, толкова по-привлекателни са те един за друг. Това е друга тема за изследване на генетиката на междуорганизмовите взаимодействия.
Къде и как да уча
Студентът може да изучава генетика на околната среда в биологичните факултети, катедрите по генетика (или дори конкретно - генетика на околната среда) на различни университети. Това могат да бъдат индивидуални специализации или магистърски програми или просто теми тезисивъзпитаници.
В допълнение към пряко специализираните, сред изучаваните дисциплини - генетични механизми на адаптация, механизми на модификационна вариабилност(това, което не е причинено нито от гени, нито от техните мутации и възниква по време на живота на организма, в зависимост от неговите условия), гени на околната среда и човешка наследствености други. Има допълнителни курсове цитогенетика популационна генетика,имуногенетика,генетика на стареенетои други също толкова интересни теми.
На практикумите те се учат да работят с моделни обекти, да планират и поставят експерименти правилно (т.е. в съответствие с поставената цел), да получават резултати и да анализират получените данни с помощта на методите на математическата статистика.
И генетиката, и екологията - и без хляб може ли?
 Не е лесно да си биолог в наши дни. Не е тайна, че на науката у нас се обръща много малко финансово внимание. Но генетиката в този смисъл имаше късмет. Призоваваме да подкрепим ентусиазма на младите генетици голям бройразлични стипендиантски програми, конкурси, грантове - както руски, така и съвместни с чуждестранни колеги. По-специално, една от най-популярните местни финансови програми са грантовете от Руската фондация за фундаментални изследвания (RFBR). Между другото, средства могат да се отпускат както за фундаментални проекти на лаборатории като цяло, така и за научни проекти на отделни млади учени, в зависимост от конкретните програми и условията на конкурсите.
Не е лесно да си биолог в наши дни. Не е тайна, че на науката у нас се обръща много малко финансово внимание. Но генетиката в този смисъл имаше късмет. Призоваваме да подкрепим ентусиазма на младите генетици голям бройразлични стипендиантски програми, конкурси, грантове - както руски, така и съвместни с чуждестранни колеги. По-специално, една от най-популярните местни финансови програми са грантовете от Руската фондация за фундаментални изследвания (RFBR). Между другото, средства могат да се отпускат както за фундаментални проекти на лаборатории като цяло, така и за научни проекти на отделни млади учени, в зависимост от конкретните програми и условията на конкурсите.
Генетикът на околната среда може да се занимава не с фундаментална наука, а с приложни дейности. Всичко ще зависи от това къде ще попадне на работа. Ако тестовете и изследванията се извършват в държавни и частни фирми и лаборатории, които не се занимават с наука като такава, частните компании могат да предложат доста добри печалби. Броят на тези места обаче е ограничен. От друга страна, ако имате първоначални средства, можете да създадете собствена компания или независима експертна лаборатория - може би като обедините усилията си, например, с химици-аналитици.
Въпреки това, голямата чест на екологичните генетици, които искат да работят по специалността си, все още остава в науката. Постоянно се провеждат множество конференции и училища за обмен на информация и установяване на контакти между млади учени - чудесен начин да намерите перспективи: по този начин можете да се натъкнете на интересни темии развитие, научете за стажове. Наскоро започна редовно да се провежда училище по екологична генетика, а организаторите на това училище бяха именно активистите на катедрата по генетика и развъждане на Санкт Петербургския държавен университет. За радиационните генетици, Училището на радиационните биолози се провежда ежегодно в Обнинск, много интересно и полезно събитие, организирано от Центъра за медицински радиологични изследвания в Обнинск.
Разбира се, международните конференции откриват специални перспективи за нас. И така, няколко мои познати създадоха полезни контакти в различни страни и получиха покана за работа в чужбина (например едно момиче сега работи в една от лабораториите в Германия). Има например съвместни руско-германски проекти за радиологични изследвания.
Полезни хора
Така че да бъдеш или да не бъдеш? И сега всеки сам решава. От свое име мога да ви уверя, че екологичната генетика и всички нейни раздели, които описах, са много интересни, изключително полезни и много обещаващи. Не говоря за факта, че като всяка наука, екологичната генетика изучава това, което е около нас, само че в много по- важен аспект- аспектът на пряко влияние върху нас. В края на краищата нашият свят е всичко, с което влизаме в контакт и взаимодействаме всеки ден.
И накрая, ще посея семе надежда в душите на тези, които биха искали да се занимават с наука (по-специално с генетика на околната среда), но които все още се глождят от въпроса за финансовите перспективи. За съжаление, поради ниските заплати, в наше време в науката се занимават само заинтересовани ентусиасти. Малко са тези. От друга страна всяка година у нас има все повече икономисти, юристи и представители на други престижни и много добре платени професии. Всичко това - засега... Представете си какво ще се случи след 10-15 години, когато мъдрите, уважавани, но, уви, не вечни по-старото поколениедори онези съветски учени ще отидат на заслужена почивка ... Ученият ще стане рядък вид, включен в Червената книга. Но държавата наистина има нужда от наука. И за да се привлекат хора в тази област, ще започне (да, изглежда, че вече започва - заплатата на служителите на RAS е увеличена 2 пъти) да насърчава науката в рублата. Да си научен работник ще стане престижно не само заради общественото уважение към умствения труд, но и във финансов смисъл.
Кой ще заеме мястото на по-старото поколение учени? Вие. Докато "екстра" юристите и икономистите няма да знаят къде да се поставят...
Отзиви, коментари и дискусии
Генетиката е наука за моделите на наследствеността и вариациите. В наше време генетиката играе една от най-важните важни ролине само в медицината, но и в селското стопанство.
Кой е генетик?
Генетикът е медицински специалист, който се занимава с диагностика, лечение и профилактика на патологични процеси, причинени от наследствена предразположеност. Най-често хората търсят съвет от генетик на етапа на планиране на дете или ако човек има съмнение за наследствено заболяване.
В случай, че двойката е родствена и планира или вече е заченала дете, консултацията и наблюдението от генетик е просто задължително.
Какво влиза в компетентността на генетиката?
Всички заболявания, които могат да се дължат на наследствена предразположеност или да са причинени от родство между близки роднини, попадат в компетенциите на генетика.
В допълнение, генетикът може да изчисли степента на риск от развитие на определено заболяване при дете, при условие че и двамата родители или един от тях са носители. В този случай лекарят задължително провежда разговор с родителите, като им обяснява всички фактори, рискове и развитието на патологичния процес в бъдеще.
Трябва да се отбележи, че генетикът не лекува нито един орган. Специалистът работи за идентифициране на заболяването като цяло, по отношение на целия организъм.
Какви заболявания лекува генетикът?
В сферата на компетентност на този специалист е огромен брой патологични процеси. Някои от тях са изключително редки. Най-честите заболявания включват следното:
- патологии, които имат доминиращ, рецесивен Х-свързан тип наследяване;
- геномика;
- синдроми различни видове(, дисомия, котешки вик);
- умствена изостаналост;
- генетичното предразположение на бебето към алкохолизъм, употреба на наркотици, никотин;
- различни видове мутации.
В допълнение, генетикът може да изготви родословие и да изчисли степента на риск от развитие на генетично заболяване при дете на етапа на зачеване.
Кога трябва да посетите генетик?
Консултацията с този специалист е задължителна на етапа на планиране на дете, при условие че в семейството е имало случаи на тежки наследствени патологии. Особено трябва да обърнете внимание на това, ако в семейството вече е родено дете, с някакво генетично заболяване или с патология с неизвестна етиология.
Все пак трябва да се отбележи, че консултацията с генетик няма да е излишна, дори ако няма видими причини за безпокойство. С помощта на съвременни диагностични методи може да се открие сериозна патология още на етапа на първия триместър на бременността. Посещението при генетик е задължително, ако ултразвукът установи отклонение в развитието на плода.
Необходимо е да се вземе предвид фактът, че диагнозата на специалист не винаги може да се счита за изречение. Много патологични процеси, дори тези с наследствена предразположеност, могат да бъдат коригирани или сведени до минимум.
Също така трябва да се свържете с генетиката, ако са верни следните фактори:
- жената ражда само мъртви деца или бременността завършва със спонтанен аборт;
- V женена двойкакогато жената е на 35 или повече години;
- лице, което е предразположено към генетични заболявания и планира дете;
- хора, които имат патологично влошаване на умствената дейност с възрастта;
- двойки, които са кръвни роднини.
Как работи генетиката
Работата на лекаря с пациентите започва с фамилна анамнеза. За да се изключат етиологични фактори от различна форма, пациентът първоначално се изследва от определени специалисти.
Едва след като генетикът разполага с резултатите от изследването и пълната фамилна анамнеза, се назначава диагностична програма.
Методи за генетични изследвания
В своята работа специалистът използва следните диагностични методи:
- скрининг на генетичен тип;
- ДНК диагностика;
- изследване на хромозоми;
- кариотип.
Ако говорим за патология на плода, тогава се предписват допълнителни методи за изследване:
- биопсия на материал от матката;
- биохимичен маркер на майката;
Що се отнася до инвазивните методи, те се предписват само в най-крайните случаи. Това се дължи на факта, че такива инструментални анализи могат да повлияят на здравето на детето.
Навременното насочване на двойката към този специалист може да помогне за предотвратяване на развитието на тежка патология при дете ранна фазаразвитие на плода. Правилното планиране на бебето позволява, ако не да изключи, тогава да сведе до минимум риска от развитие на сериозни заболявания и усложнения. Последното засяга не само самото дете, но и неговата майка. Трябва също да се отбележи, че в случая става дума не само за физическо здравебебето и родителите, но и за психологическите.



